Факторы, влияющие на краевую резорбцию кости и неприживление имплантатов, установленных врачами-интернами: однолетнее, проспективное, когортное исследование
Жан Мария Рагуччи1,*, Мария Гиральт-Хернандо1 , Ирен Мендез-Манйон1, Ориоль Канто-Навес 2 , Федерико Хернандез-Альфаро1,3
1. Кафедра хирургической стоматологии и челюстно-лицевой хирургии, Международный университет Каталонии (UIC), 08017 Барселона, Испания; mariagiralth@gmail.com (M.Г.-Х.); manjon.irene@gmail.com (И.M.-M.); h.alfaro@uic.es (Ф.Х.-A.)
2. Кафедра ортопедической стоматологии, Международный университет Каталонии (UIC), 08017 Барселона, Испания; oriolcanto@uic.es
3. Институт челюстно-лицевой хирургии, Медицинский центр Текнон, 08022 Барселона, Испания
* Адрес для переписки: gian1@uic.es Materials 2020, 13, 4511; doi:10.3390/ma13204511
Статья получена: 18 сентября 2020 г.; Статья принята 8 октября 2020 г.; Статья опубликована: 12 октября 2020 г.
Реферат:
Состояние проблемы: Подавляющее большинство клинической документации, посвященной оценке успеха лечения с использованием дентальных имплантатов и их выживаемости, опубликованное в литературе, выпущено группами опытных специалистов в университетских условиях, включая строгие критерии отбора пациентов, или соответствующими врачами частной практики. Напротив, исследования, посвященные установке и протезированию с опорой на имплантаты врачами-интернами с небольшой клинической практикой, крайне немногочисленны. Цель: Зарегистрировать частоту случаев неприживления имплантатов и идентифицировать факторы, влияющие на краевую резорбцию кости (КРК) и неприживления имплантатов и при установке, и протезировании с опорой на имплантаты врачами-интернами с небольшой клинической практикой, с последующим однолетним наблюдением. Материалы и методы: Данное проспективное когортное исследование было проведено в Международном университете Каталонии с участием пациентов, которым была запланирована дентальная имплантатация. Опытный преподаватель определял план лечения в соответствии с потребностями каждого пациента, подписавшего информированное согласие на лечение. Все хирургические вмешательства и протезирование осуществляли врачи-интерны. Частоту неприживления имплантатов, влияние факторов на их неприживления, а также КРК изучали с учетом 24 переменных, касающихся здоровья пациента, участка полости рта, характеристик имплантата и зубного протеза. Риск несостоятельности имплантата анализировали с использованием простой модели бинарной регрессии с моделями равенств генерализованных выражений (РГВ), с получением нескорректированных отношений шансов (ОШ). Взаимосвязь между КРК и другими независимыми переменными была изучена на модели простой линейной регрессии, с оценкой на моделях РГВ и с критерием Хи2 Уолда. Результаты: Врачами-интернами установлено в общей сложности 130 дентальных имплантата с последующим протезированием с опорой на эти имплантаты. Отмечалось неприживление 5 имплантатов до протезирования и ни одного после установки ортопедических конструкций; выживаемость и уровень успеха составили 96,15 % и 94,62 % соответственно. Ни одна из изученных переменных не оказывала достоверного влияния на выживаемость имплантатов. При контрольном обследовании спустя один год средне отклонение (СО) КРК составило 0,53 (0,39) мм. На КРК достоверно влияли следующие независимые переменные: диабет, глубина установки имплантата. Ширина кератинизированной десны (КД) и глубина зондирования (ГЗ) более 3 мм отмечены как хорошие индикаторы КРК, каждый дополнительный миллиметр глубины зондирования соответствовал дополнительной КРК 0,11 мм. Вывод: Уровни выживаемости дентальных имплантатов и успеха лечения с их помощью при установке и протезировании врачами- интернами с небольшим опытом работы были высокими при последующем наблюдении через один год. Не обнаружены факторы, влияющие на неприживление имплантатов. При этом несколько факторов достоверно влияли на КРК: диабет, глубина установки имплантата, ГЗ и ширина КД. Клиническое значение: Уровни выживаемости дентальных имплантатов и успеха имплантологического лечения и протезирования врачами-интернами с небольшим опытом работы были высокими при последующем однолетнем наблюдении, сходными с таковыми для опытных специалистов. Факторы, влияющие на неприживление имплантатов, не были установлены; при этом, несколько факторов достоверно влияли на КРК – диабет, глубина установки имплантата, ГЗ и КД.
1. Введение
Дентальная имплантация стала прогнозируемым методом лечения пациентов с частичной и полной адентией; документально подтверждена долговременная выживаемость имплантатов, составляющая 95,2 % [1]. В отличие от выживаемости имплантатов, успех имплантологического лечения определен во взаимосвязи от величины краевой резорбции кости (КРК), возникающей со временем [2]. В литературе описано несколько этиологических факторов, влияющих на КРК, включающих, среди прочего: количество кератинизированной десны (КД), толщину десны, высоту абатмента ортопедической конструкции, накопление зубного налета, а также окклюзионную перегрузку [2,3]. Курение и наличие пародонтита в анамнезе также продемонстрировали более высокую восприимчивость пациентов к периимплантиту [4,5]. Предложен ряд стратегий для уменьшения или стабилизации КРК, например, принцип переключения платформы для соединения «имплантат-абатмент» [6–8]; использование ортопедических абатментов, таких как титановое основание, или многокомпонентных абатментов размером > 2 мм [9–11]; достижение толщины слизистой > 2 мм при установке имплантата [12,13]. В подавляющем большинстве случаев в литературе документированы выживаемость, успех и КРК для имплантологического лечения, опубликованные группами опытных специалистов, в университетских условиях со строгими критериями отбора пациентов, или в частных стоматологических клиниках [1–8]. В настоящее время пациентам во всем мире устанавливают несколько миллионов имплантатов ежегодно; большинство из них устанавливают врачи, имплантологическое лечение для которых не является рутинной деятельностью [14]. Опубликованная литература по дентальным имплантатам формирует картину оптимальной эффективности, которая может быть достигнута при установке имплантатов хорошо обученными и опытными врачами [1]. Это может оказаться не репрезентативным для состояния имплантологического лечения, проводимого в частных стоматологических практиках менее опытными специалистами. В ретроспективном исследовании, посвященном сравнению опытных и неопытных хирургов, Preiskel и Tsolka продемонстрировали, что опыт оказывал преобладающее влияние на вероятность неприживления имплантатов [15]. Позднее, Sendyk соавт. [16] сделали заключение, что на неприживление имплантатов достоверно влиял опыт хирурга и количество установленных им имплантатов (менее или более 50). В набирающих популярность методах немедленного протезирования с опорой на имплантаты Ji и соавт. [17] обнаружили повышенный риск потери имплантата при его установке хирургами с менее чем пятилетним опытом (12,2 %), по сравнению с 2,4 % при работе более опытных врачей. Таким образом, целью данного проспективного исследования была оценка успеха, выживаемости и КРК вокруг имплантатов (C1, MIS Implants Technologies, Шломи, Израиль), установку и протезирование на которых осуществляли не имеющие клинического опыта врачи- интерны, без применения строгих критериев отбора пациентов. Кроме того, изучены другие параметры и их корреляция с состоянием здоровья пациента, местными факторами, хирургическими и ортопедическими протоколами.
2. Материалы и методы
2.1. Дизайн исследования
Данное проспективное исследование было проведено на кафедре хирургической стоматологии и челюстно-лицевой хирургии Международного университета Каталонии после одобрения комиссией университета по биоэтике (CIR-ECL-2015-06). В исследование были включены пациенты, нуждающиеся в имплантологическом лечении, которым были установлены имплантаты С1 с января 2016 года по январь 2017 года.
2.2. Критерии включения/невключения
Были включены любые показания, включая установку одиночных коронок, частичных несъемных протезов и полных зубных протезов. До включения пациента цель и процедуры в исследовании были подробно разъяснены пациенту. Критерии включения: (a) Пациенты старше 18 лет, нуждающиеся в имплантологическом лечении, (b) хорошее общее/системное состояние здоровья (тип I, II ASA), (c) пациенты, готовые осуществлять все визиты в рамках исследования, (d) пациенты, подвергшиеся или нуждающиеся в операции направленной костной регенерации, горизонтальной или вертикальной, с использованием резорбируемых мембран или трансплантатов в виде блока или без них, (e) пациенты после синус-лифтинга, (f) адекватная гигиена полости рта с показателем индекса налета во всей полости рта (ИНВПР) < 15 % до операции, (g) отсутствие неконтролируемого пародонтита, (h) дача письменного информированного согласия. Критерии невключения: (a) пациенты с соответствующим медицинским анамнезом, в котором любая перенесенная операция, заболевание, состояние или медикаментозное лечение могли бы скомпрометировать заживление твердых и мягких тканей (неконтролируемый диабет, нарушение функции печени, заболевание иммунной системы), (b) прием иммунодепрессантов, (c) вредные привычки, за исключением курения, которые могли бы скомпрометировать или нарушить заживление, (d) пациенты, подвергавшиеся химиотерапии или лучевой терапии в течение предыдущих 5 лет, включая область головы и шеи, (e) терапия кортикостероидами или любыми другими препаратами, которые могли бы повлиять на послеоперационное заживление и/или остеоинтеграцию, (f) лечение бисфосфонатами или препаратом Denosumab (Prolia®, Amgen Europe B.V. Breda(NL) Нидерланды), (g) неспособность или нежелание приходить на визиты для наблюдения, (h) отказ подписать форму информированного согласия.
2.3. Хирургическая методика
Все хирургические и ортопедические процедуры были проведены в университетской стоматологической клинике 24 врачами-интернами, только закончившими обучение на стоматологическом факультете; все они были в возрасте от 24 до 27 лет. До установки имплантатов диагностический протокол включал изготовление диагностической модели для получения рентгенологического шаблона. Проводили конусно-лучевую компьютерную томографию (iCAT®, Imaging Science International, Хэтфилд, штат Пенсильвания, США) целевой области с соответствующим рентгенологическим шаблоном для получения трехмерного изображения, а также для выбора и трехмерного позиционирования имплантата. Осуществляли последовательность препарирования с использованием каждой фрезы включая финальную, поставляемую с каждым имплантатом, в соответствии с рекомендациями производителя. Основной характерной чертой имплантатов C1 является их коническая форма, наличие микроколец в области шейки, а также конструкция с двойной резьбой; следует отметить реализацию принципа переключения платформы и коническое соединения с углом 12°. Поверхность имплантатов C1 подвергается пескоструйной обработке и кислотному протравливанию. В зависимости от величины моментного усилия при установке, зарегистрированного на хирургическом микромоторе (Implantmed W&H, Burmoos (AU) Австрия), превышавшего или не превышавшего 35 Н·см, устанавливали формирующий абатмент десны, или заглушку. Одноэтапную схему лечения применяли, устанавливая формирующий десну абатмент и формирование лоскутов одиночным швами; при двухэтапном лечении устанавливали заглушку и ушивали лоскут мягких тканей наглухо. Пациентам назначали антибиотик (875/125 мг амоксициллин/клавулановая кислота, 3 раза в сутки в течение 7 дней; в случае аллергии на антибиотики пенициллинового ряда назначали 300 мг клиндамицина каждые 6 ч в течение 7 дней) и противоболевое противовоспалительное лечение (600 мг ибупрофена 3 раза в сутки); полость рта обрабатывали хлоргексидином (0,12 %) (Dentaid. PerioAid 0,12 %) 2 раза в сутки в течение 2 недель. Через 7 дней пациенты приходили на визит для снятия швов; следующий визит был назначен через 1 месяц. Через 3 месяца заживления (как в области нижней, так и в области верхней челюсти) контроль остеоинтеграции осуществляли как клинически, так и рентгенологически. Ортопедический этап лечения (T1) включал установку несъемных частичных металлокерамических протезов на многокомпонентный абатмент, а также установку одиночных металлокерамических коронок, фиксируемых на титановое основание.
2.4. Переменные и измерения в исследовании
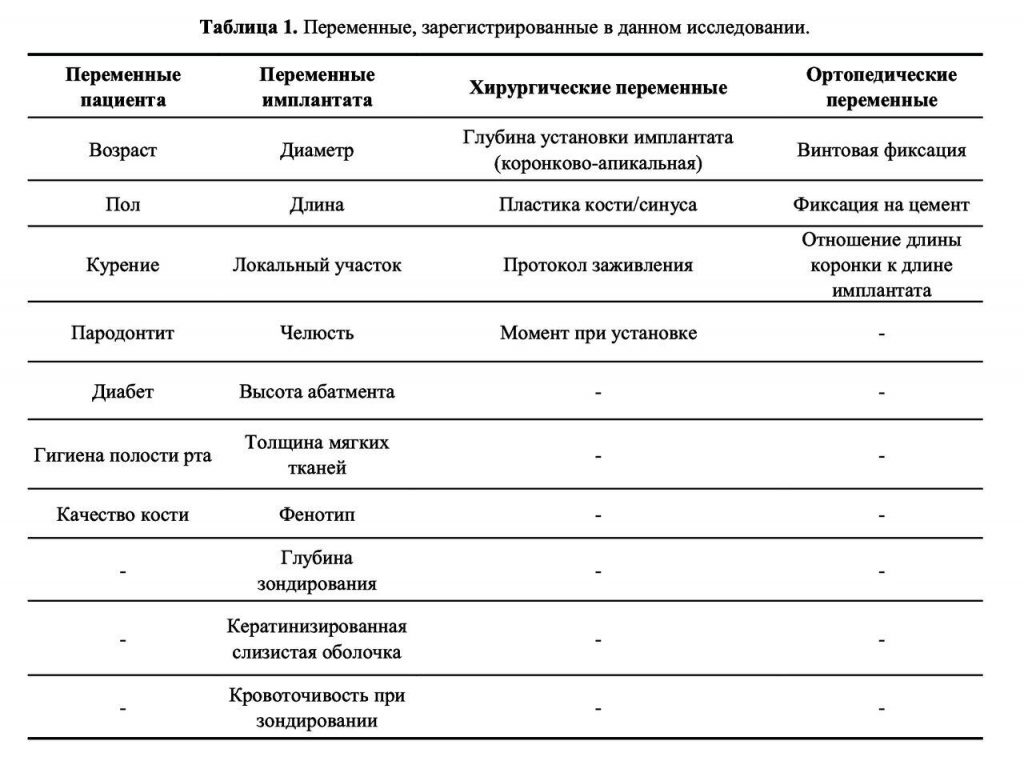
Регистрировали демографические параметры участников исследования: возраст, пол, привычка курения, данные медицинского анамнеза. Регистрировали 24 переменные в соответствии с характеристиками пациента, имплантата, зоны операции, ортопедических исходов/переменных (Таблица 1). Уровень успеха лечения вычисляли в соответствии с критериями Buser и соавт. [18], модифицированными Albrektsson и Zarb [19].
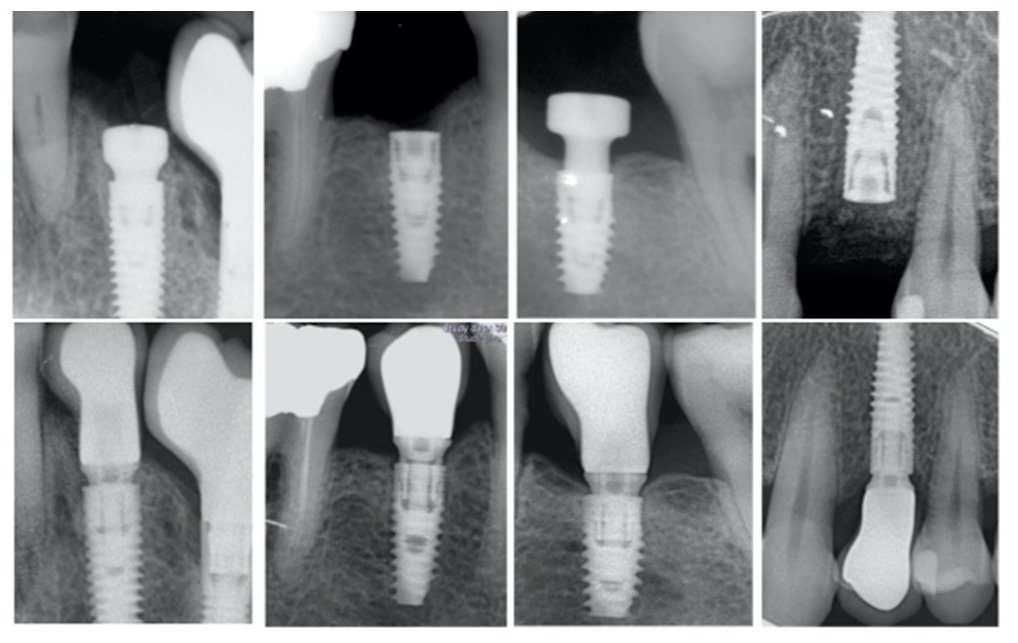
Прицельные рентгенограммы каждого имплантата получали с использованием интраоральной стоматологической пленки, используя пластмассовый указатель в параллельной технике, непосредственно после имплантации, в момент протезирования и через один год. Измерения проводили с использованием программного обеспечения Image J (10.8.0_172, Национальный институт здоровья, штат Мериленд, США); внутреннюю калибровку осуществляли по диаметру имплантата на уровне его шейки. В каждой временной точке расстояние от плеча имплантата до первого контакта «кость-имплантат» измеряли с мезиальной и дистальной стороны. Для вычисления КРК с каждой стороны использовали различие между исходным значением и значением в определенной временной точке. После этого для каждого имплантата определяли среднее значение для двух измерений. (Рис. 1).
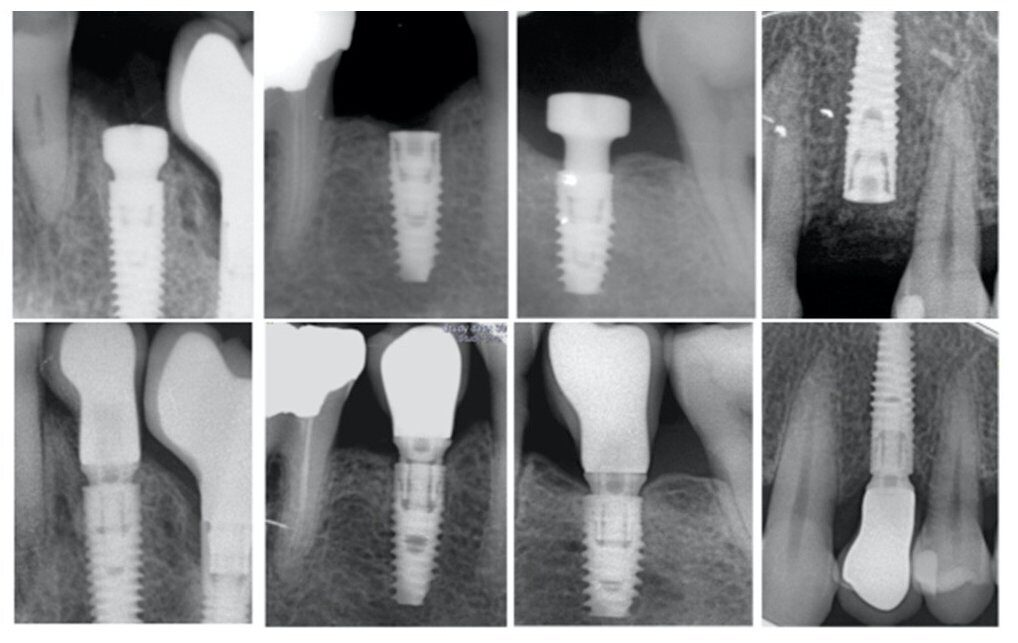
Рис. 1. Прицельные рентгенограммы с использованием интраоральной стоматологической пленки и пластмассового указателя, полученные в параллельной технике, для анализа краевой резорбции кости (КРК) от исходного значения до значения спустя 1 год.
Клинические параметры окружающих имплантат тканей оценивали для трех участков (мезиальный, щечный и дистальный) с помощью пародонтологического зонда (UNC 15, HuFriedy):
— Глубину зондирования (ГЗ) в миллиметрах измеряли от края десны, окружающей имплантат, до основания борозды вокруг имплантата.
— Кровоточивость при зондировании (КПЗ) определяли как наличие или отсутствие кровотечения через 15 с после осторожного зондирования.
— Ширину кератинизированной десны (КД) в миллиметрах измеряли с помощью пародонтологического зонда посередине щечной стороны имплантата от свободного края десны до мукогингивального соединения. Кроме того, измерения КД разделили на две группы: группа 1 – КД ≥ 2 мм и группа 2 – КД < 2 мм.
— Глубина установки имплантата: В день операции получали прицельную рентгенограмму для получения информации о глубине установки имплантата (по его проксимальным сторонам).
Кроме того, регистрировали расположение имплантата (верхняя или нижняя челюсть, фронтальный или боковой участок), а также тип ортопедической конструкции, опирающейся на имплантат – одиночная коронка (ОК) или несъемный частичный протез (НЧП). Два исследователя (Ж.M.Р. и M.Г.-Х.) независимо оценивали клинические параметры через один год наблюдения. При возникновении расхождений, показатели обсуждали с третьим лицом (Ф.Х.-A.). Клинические и рентгенологические обследования проводили по одной и той же методике в начале исследования (T0), при установке протеза (T1) и через 1 год наблюдения (T2).
2.5. Статистические методы
Данные описательной статистики, анализируемые на уровне участника и имплантата: среднее значение (стандартное отклонение), минимум, максимум, медиана – для непрерывных переменных; абсолютные частоты и процентные доли – для категорийных переменных. Вероятность неприживления на уровне имплантата на основе каждого из независимых факторов и ковариат определяли на модели простой бинарной логистической регрессии с моделями равенств генерализованых выражений (РГВ) с получением нескорректированых отношений шансов (OШ), как функцию факторов профиля. Взаимосвязь между КРК и независимыми переменными была изучена на модели простой линейной регрессии, с оценкой на моделях РГВ и с критерием Хи2 Уолда. Переменные были категоризованы как значимые (p < 0,05) или релевантные (p < 0,1), предложена множественная модель для получения полностью скорректированных коэффициентов.
3. Результаты
Исходно, 130 имплантатов были установлены 67 пациентам (43 женщины и 24 мужчины), средний возраст которых составил 48,6 (10,2) лет; 12,1% из них курили менее 10 сигарет в день; у 39,4% в анамнезе был пародонтит, контролируемый на момент установки имплантата; 6,1% пациентов страдали от сахарного диабета. 37 имплантатов (28,5%) были установлены во фронтальном участке, 93 (71,5%) – в боковом; 44,6% имплантатов были установлены на верхней челюсти.
3.1. Выживаемость имплантатов
Перед протезированием 5 имплантатов у 5 пациентов оказалисьнеприживленными (2 женщины (3,9 %) и 3 мужчины (3,8 %); ни одиного в последующем. Выживаемость имплантатов составила 96,15 % с 95 % ДИ (91,3–98,7 %); неприживаемость имплантатов зарегистрирована у 7,5 % пациентов: 5 % курильщиков и 2,8 % некурящих. Неприживаемость имплантатов у пациентов с пародонтитом в анамнезе, или без него составила 4,6 % и 1,6 %, соответственно (Таблица 2).
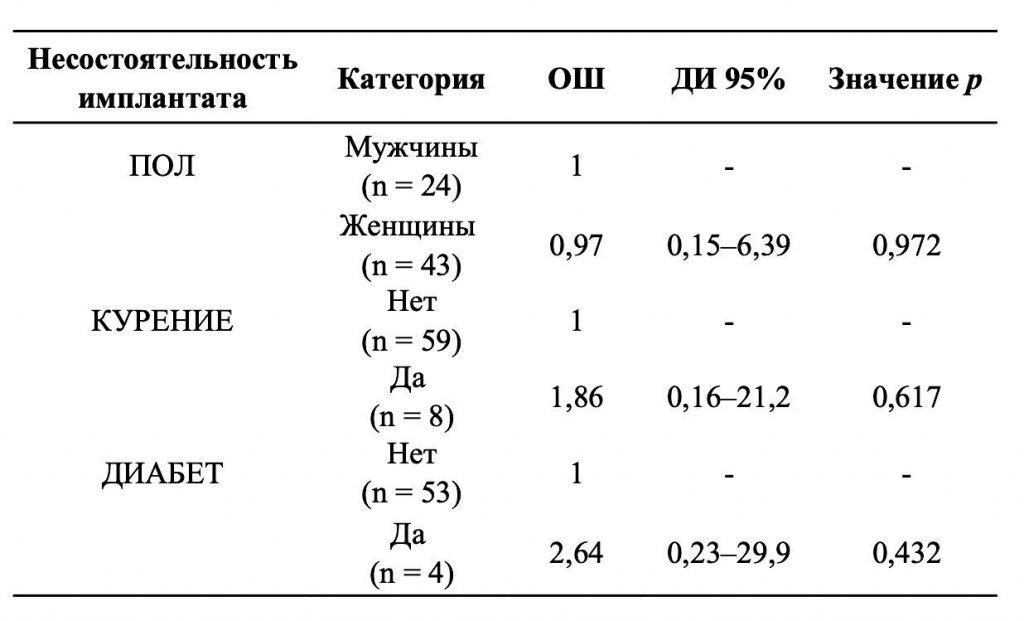

Таблица 2. Вероятность несостоятельности в соответствии с независимыми переменными: Критерий Хи [2] Уолда позволил построить простую бинарную модель логистической регрессии. Отношение шансов (ОШ) не могло быть вычислено в связи с отсутствием случаев несостоятельности. Ни одна из переменных не оказывала статистически достоверного влияния на несостоятельность, отмечена лишь тенденция для одной переменной (p < 0,143).
Не обнаружен ни один параметр, статистически достоверно влиявший на выживаемость имплантатов (Таблица 2). При этом обнаружена релевантная взаимосвязь между выживаемостью и положением имплантата (во фронтальном или боковом участке); риск неприживаемости имплантатов, расположенных в боковом участке, был в 4 раза ниже, чем во фронтальном (p = 0,143) (Таблица 2).
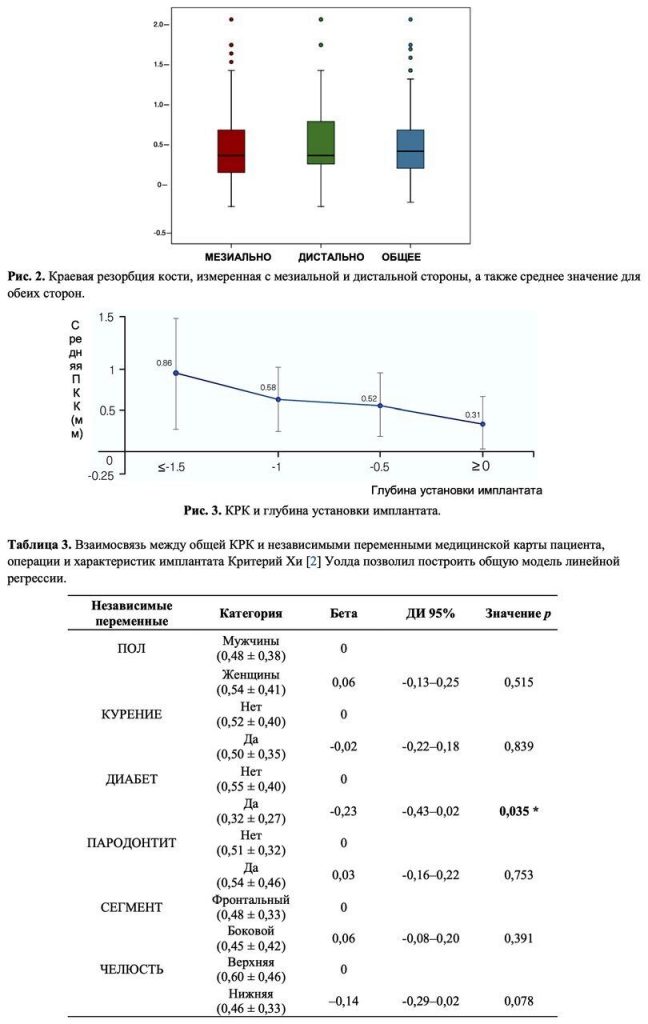
3.2. Краевая резорбция кости и успех имплантологического лечения
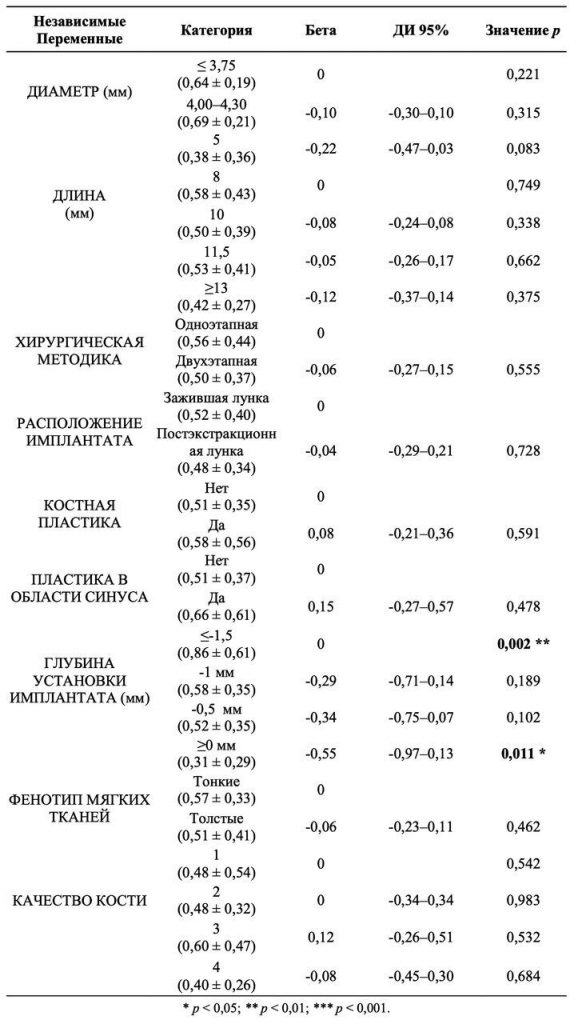
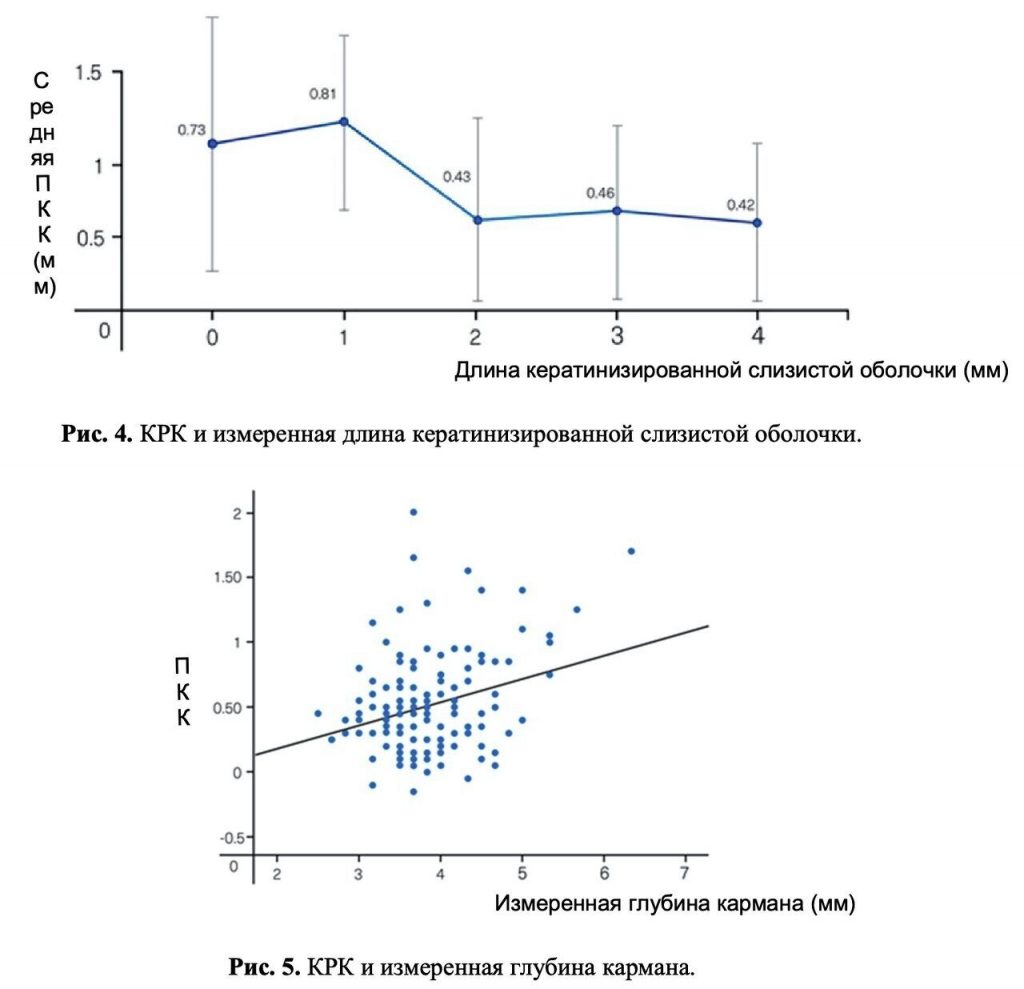
КРК вычисляли с мезиальной и дистальной стороны (Рис. 1) и усредняли для каждого имплантата. Средняя КРК с мезиальной и дистальной стороны составила 0,48 (0,42) и 0,56 (0,43) мм соответственно; усредненная КРК с обеих сторон составила 0,53 (0,39) мм (Рис. 2). Уровень успеха лечения составил 94,62 %. На КРК статистически достоверно влияло наличие у пациентов диабета, 0,55 (0,40) против 0,32 (0,27) мм, p = 0,035, для пациентов без диабета и пациентов с контролируемым диабетом соответственно. Более глубокая установка имплантата (измерение на аппроксимальных поверхностях) приводила к увеличению резорбции кости (p = 0,003) (Рис. 3); каждый миллиметр глубины установки увеличивал КРК на 0,28 мм. На КРК влиялапротяженность КД, измеренная через один год наблюдения (p = 0,004). Участки с КД < 2 мм характеризовались более выраженной потерей кости, чем участки с КД ≥ 2 мм (0,78 (0,40) против 0,45 (0,36) мм, p = 0,001, (Таблица 3, Рис. 4); каждый миллиметр менее 4 мм КД приводил к увеличению КРК на 0,08 мм.
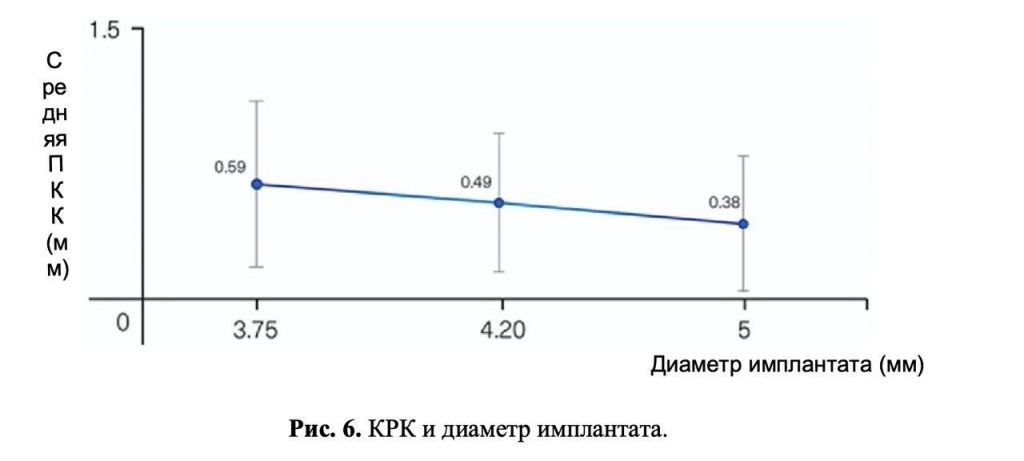
Повышенная КРК ассоциировалась с ГЗ, превышавшей 4 мм (p = 0,008); каждый дополнительный миллиметр ГЗ свыше 4 мм приводил к увеличению КРК на 0,18 мм (Рис. 5).
Значимыми параметрами, влиявшими на КРК, но без статистически достоверных отличий, были диаметр имплантата (p = 0,064) и челюсть(p = 0,078). Имплантаты более крупных диаметров характеризовались меньшей величиной КРК по сравнению с более мелкими имплантатами (Рис. 6): 0,73 (0,04) мм для Ø 3,3 мм, 0,59 (0,44) мм для Ø 3,75 мм, 0,49 (0,37) мм для Ø 4,2 мм, 0,38 (0,36) мм для Ø 5 мм. Имплантаты, установленные в области верхней челюсти, характеризовались большей величиной КРК по сравнению с имплантатами, установленными в области нижней челюсти: 0,60 (0,46) по сравнению с 0,40 (0,33) мм соответственно.
Наконец, наличие пародонтита в анамнезе (p = 0,348), курение (p = 0,617), толщина слизистой оболочки (p = 0,384), фенотип десны (p = 0,462), момент при установке (p = 0,344), высота абатмента (p = 0,146), и все ортопедические переменные (p = 0,952) не влияли на КРК (Таблицы 3 и 4).
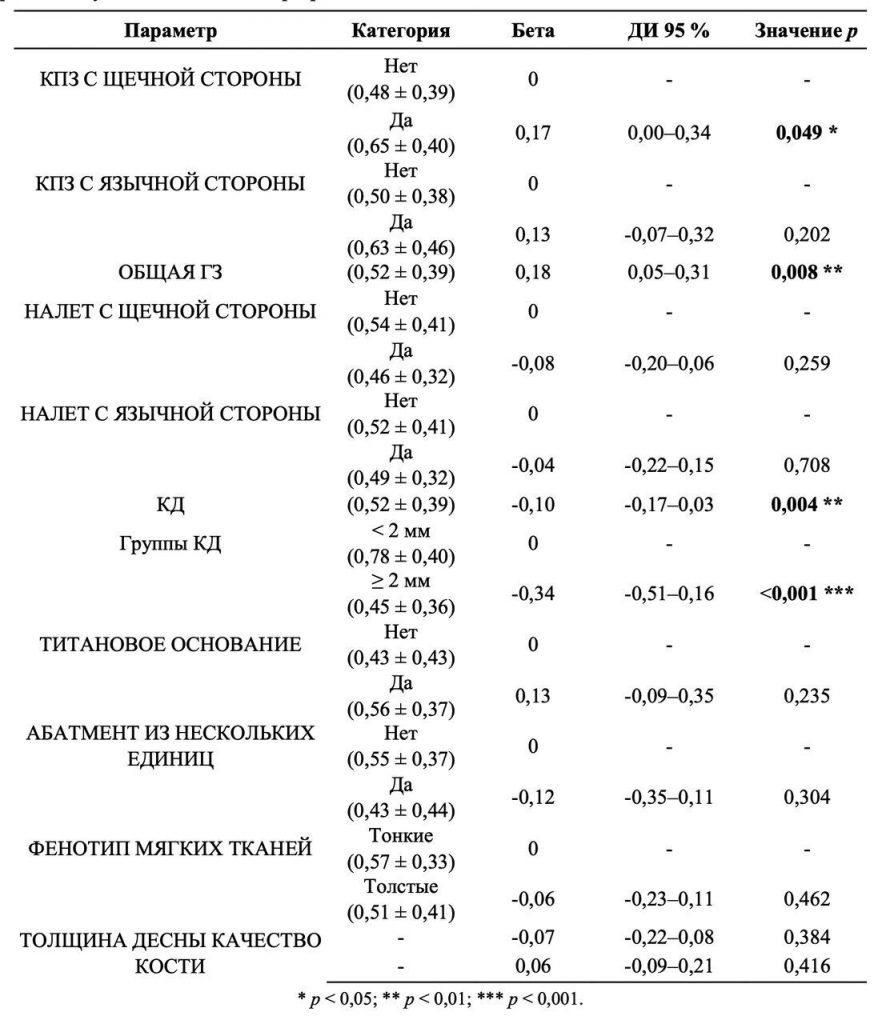
Таблица 4. Взаимосвязь между КРК и другими клиническими параметрами. Критерий Хи [2] Уолда позволил построить общую модель линейной регрессии.
4. Обсуждение
Лишь в немногих исследованиях изучена взаимосвязь между опытом хирурга и выживаемостью имплантатов [16]. Цитируемые авторы обнаружили, что обучение специалиста не являлось указанием клинических достижений; скорее, опыт установки хотя бы 50 имплантатов оказывал в этом случае детерминирующее влияние. Несмотря на то, что корреляция между опытом и частотой неудач лечения кажется интуитивной, многие другие факторы также вносят свой вклад; например, навыки хирурга, удобная для работы форма имплантата, адаптированные инструменты для препарирования, могут также повлиять на выживаемость [17]. Это является причиной опасности экстраполирования достижений при использовании одной системы имплантатов на другую. Данное проспективное когортное исследование было проведено для оценки выживаемости и уровня успеха лечения при использовании системы имплантатов С1 (MIS), установку и протезирование с опорой на которые осуществляли не имеющие опыта врачи-интерны; имплантаты являлись самонарезающими, с коническим соединением и возможностью переключения платформы. Через один год наблюдения выживаемость имплантатов и уровень успеха лечения составили 96,15 % и 94,62 % соответственно. Полученные данные сходны с результатами для выживаемости, описанными в литературе [20–22]. Более того, они хорошо сходятся с результатами одногодичного исследования [23], посвященного установке 117 имплантатов C1 у 60 пациентов опытными пародонтологами; описанные значения выживаемости и успеха лечения у этих активно частно практикующих стоматологов составили 98,3 % и 95,4 % соответственно.
Таким образом, данное исследование с 24 недавними студентами, установившими всего 130 имплантатов, показывает, что отсутствие опыта хирургов не приводило к более высокой частоте неприживления имплантатов при использовании данной системы. Возможно, присутствие опытного врача-наставника, помогавшего в планировании имплантологического лечения, может объяснить результат; в этом случае придется опираться на предположение, что неудачи являются скорее результатом недостаточного планирования, чем исключительно хирургических навыков. Также возможно, что форма имплантатов С1 является удобной в использовании в отношении препарирования и достижения первичной стабильности и прощает новичку некоторые ошибки. Ни одна из ковариат достоверно не влияла на уровень выживаемости, но отмечена тенденция, что имплантаты, установленные в боковых участках челюсти, характеризовались в четыре раза меньшей неприживаемостью по сравнению с имплантатами, установленными во фронтальном участке (p = 0,143).
Средняя КРК для имплантатов, установленных врачами-интернами, составила 0,48 (0,42) и 0,56 (0,43) мм с мезиальной и дистальной стороны соответственно. Аналогичная КРК, составившая 0,54 (0,55) и 0,52 (0,45) мм, была определена с мезиальной и дистальной стороны таких же имплантатов при их установке опытными хирургами [23]. Лишь два параметра (диабет и глубина установки имплантата) достоверно влияли на КРК. Влияние диабета на КРК было изучено в недавнем систематическом обзоре Maior и соавт. [24]; представленные данные соответствуют результатам данного исследования, описано положительное влияние на КРК, если заболевание контролируется. Следует акцентировать внимание, что критерии включения пациентов в данное исследование позволяли включать лишь пациентов с контролируемым диабетом; таким образом, заключение в отношении пациентов с неконтролируемым диабетом дать невозможно.
Субкрестальная установка имплантата вместо крестальной была предложена с целью избежать или отсрочить экспозицию шероховатой поверхности шейки имплантата в полость рта [25]. Такая стратегия может быть успешно реализована при условии ограниченной КРК и того, что кость, со временем, все же будет покрывать шероховатую поверхность шейки имплантата и защищать ее от бактериальной контаминации. Представленные данные продемонстрировали, что более глубоко установленные имплантаты имели тенденцию к увеличению КРК. Соответственно, имплантаты, установленные на 1,5 мм субкрестально, характеризовались потерей кости в среднем на 0,86 (0,61) мм через один год, но это по-прежнему обеспечивало среднюю высоту кости, защищающей шейку имплантата, составлявшую 0,64 мм. Установленные крестально имплантаты характеризовались потерей 0,31 (0,29) мм кости в среднем, но это могло означать, что шейка имплантата больше не была покрыта костью. Если такая тенденция сохранится и в будущем, субкрестальная установка может оказаться более предпочтительной с клинической точки зрения.
В предыдущих исследованиях было проведено сравнение субкрестальной и крестальной установки имплантатов; Ercoli и соавт. [26] измеряли КРК через 12–18 месяцев. Субкрестально установленные имплантаты характеризовались большей потерей кости, чем крестально установленные, но различие не было статистически достоверным. В соответствии с результатами данного исследования, цитируемые авторы сделали заключение, что субкрестальное расположение имплантата на момент операции приводит к снижению риска обнажения его резьбы [26]. Аналогично, в недавнем рандомизированном клиническом исследовании проведена оценка влияния апико-коронкового положения имплантата через три года наблюдения [27]. Не обнаружены заметные клинические различия между крестальным и субкрестальным положением в отношении глубины кармана; при этом рентгенологические параметры для крестального и субкрестального положения отличались: 53,4 % крестально установленных имплантатов характеризовались в среднем потерей 0,29 (0,35) мм кости ниже шейки имплантата. В группе субкрестально установленных имплантатов потеря кости ниже шейки имплантата была меньше, в среднем 0,09 (0,18) мм, и частота этого явления была ниже на 25,8 %, т.е. составляла приблизительно половину от таковой для крестально расположенных имплантатов. В группе субкрестально расположенных имплантатов 74,2 % из них все еще характеризовались наличием 0,89 (0,37) мм кости над шейкой имплантата; авторы сделали заключение, что субкрестально расположенные имплантаты снижали экспозицию шероховатой поверхности на 88 % по сравнению с крестально расположенными имплантатами. Следует отметить, что не обнаружено четкой взаимосвязи между обнажением шероховатой поверхности и кровоточивостью при зондировании, хотя и выявлена определенная статистическая тенденция (p = 0,135) [27]. С другой стороны, в систематическом обзоре Valle и соавт. [28] обнаружили достоверно меньшую КРК для имплантатов, установленных субкрестально, всего на 0,18 мм. Ограничения данного исследования, а также других исследований, связаны с тем, что все данные о кости направлены на проксимальные стороны имплантата; они не учитывают явления, происходящие в области щечной кортикальной пластинки, которая является критически важной для поддержки и сохранения краевой десны со временем.
Значение КД в сохранении здоровья окружающих имплантат тканей и КРК характеризовалось определенной противоречивостью. В ряде исследований показаны более высокие индексы налета и более выраженное воспаление окружающих имплантат тканей на участках с КД < 2 мм [29–31]. Кроме того, некоторые авторы предположили, что наличие зоны KД ≥ 2 мм является необходимым для предотвращения прогрессирования КРК и сохранения здоровья окружающих имплантат тканей со временем [32–34]. С другой стороны, в аналитических статьях предоставлены ограниченные доказательства в поддержку необходимости широкой зоны прикрепленной кератинизированной десны вокруг имплантата для поддержания его здоровья и стабильности тканей. [35,36]. Полученные авторами результаты дают основание полагать, что через один год потеря кости может быть незначительно более выражена на участках с KД < 2 мм при сравнении с участками с KT > 2 мм, 0,78 (0,40 ) против 0,45 (0,36) мм (p < 0,001) соответственно. Аналогичная тенденция обнаружена Pellicer-Chover и соавт. [25] для субкрестально установленных имплантатов через три года наблюдения. Влияние других переменных, описанных в литературе, как влияющих на КРК – толщины слизистой и высоты абатмента [9–13,37–41], – не было обнаружено в данной группе пациентов и участков имплантации. Следует отметить, что влияние толщины слизистой и высоты абатмента на КРК систематически не изучалось, и причины таких несоответствий не вполне понятны [37,42,43].
5. Выводы
С учетом ограничений данного краткосрочного когортного исследования, можно сделать следующие выводы:
1. Частота неприживаемости имплантатов С1, установку и протезирование на которых осуществляли не имеющие опыта врачи-интерны, при последующем однолетнем наблюдении была низкой (3,6 %) и сравнимой с данными, полученными опытными врачами.2. Не обнаружены факторы, связанные с недостаточным опытом врачей-интернов, влияющие в неприживаемость имплантатов и КРК.
3. Установлено несколько факторов, оказывающих влияние на КРК, например, диабет, глубина установки имплантата, ГЗ и КД, Напротив, толщина десны и высота ортопедического абатмента не отмечались среди имеющих значение факторов.
Вклад авторов: Обработка данных: И.M.-M.; Исследование: Ж.M.Р. и M.Г.-Х.; Наблюдение: O.К.-Н.; Написание статьи, рецензирование и редактирование: Ф.Х.-A. Все авторы прочли и дали согласие на публикацию рукописи.
Финансирование: Данное исследование финансировалось компанией MIS Implants Technologies, Шломи, Израиль. Номер гранта: CIR- ECL 2015-06.
Конфликты интересов: Авторы указали отсутствие конфликтов интересов.
Ссылки
1. Roccuzzo, M.; Bonino, L.; Dalmasso, P.; Aglietta, M. Long-term results of a three arms prospective cohort study on implants in periodontally compromised patients: 10 year data around sandblasted and acid etched surface. Clin. Oral Implants Res. 2014, 25,1105-1112. [CrossRef] [PubMed]
2. Sicilia, A.; Quirynen, M.; Fontolliet, A.; Francisco, H.; Friedman, A.; Linkevicius, T.; Lutz, R.; Meijer, H.J.; Rompen, E.; Rotundo, R.; et al. Long-term stability of peri-implant tissues after bone or soft tissue augmentation. Effect of zirconia or titanium abutments on peri-implant soft tissues. Summary and consensus statements. The 4th EAO consensus conference. Clin. Oral Implants 2015, 26,148-152. [CrossRef]
3. Galindo-Moreno, P.; Le.n-Cano, A.; Ortega-Oller, I.; Monje, A.; O’Valle, F.; Catena, A. Marginal bone loss as success criterion in implant dentistry: Beyond 2 mm. Clin. Oral 2015,26, 28-34. [CrossRef] [PubMed]
4. Levin, L.; Hertzberg, R.; Har-Nes, S.; Schwartz-Arad, D. Long-term marginal bone loss around single dental implants affected by current and past smoking habits. Implant Dent. 2008,17, 422-429. [CrossRef] [PubMed]
5. Levin, L.; Ofec, R.; Grossmann, Y.; Anner, R. Periodontal disease as a risk for dental implant failure over time: A longterm historical cohort study. J. Clin. Peridontol. 2011, 38, 732-737. [CrossRef]
6. Prosper, L.; Redaelli, S.; Pasi, M.; Zarone, F.; Radaelli, G.; Gherlone, E.F. A randomized prospective multi-center trial evaluating the platform switching technique for the prevention of post-restorative crestal bone loss. Int. J. Oral Maxillofac. Implants 2009, 24, 299-308. [PubMed]
7. Santiago, J.; Batista, V.; Verri, F.; Hon.rio, H.; De Mello, C.; Almeida, D.; Pellizzer, E.P. Platform switching implants and bone preservation: A systematic review and meta-analysis. Int. J. Oral Maxillofac. Surg. 2016, 45, 332-345. [CrossRef]
8. Hsu, Y.; Lin, G.; Wang, H. Effects of platform-switching on peri-implant soft and hard tissue outcomes: A systematic review and meta-analysis. Int. J. Oral Maxillofac. Implants 2017, 32, 9-24. [CrossRef]
9. Blanco, J.; Pico, A.; Caneiro, L.; N.voa, L.; Batalla, P.; Mart.n-Lancharro, P. Effect of abutment height on interproximal implant bone level in the early healing: A randomized clinical trial. Clin. Oral Implants Res. 2018, 29,108-117. [CrossRef]
10. Pico, A.; Mart.n-Lancharro, P.; Caneiro, L.; N.voa, L.; Batalla, P.; Blanco, J. Influence of abutment height and implant depth position on inter-proximal peri-implant bone in sites with thin mucosa: A 1-year randomized clinical trial. Clin. Oral Implants Res. 2019, 30, 595-602. [CrossRef]
11. Galindo-Moreno, P.; Le.n-Cano, A.; Monje, A.; Ortega-Oller, I.; O’Valle, F.; Catena, A. Abutment height influences the effect of platform switching on peri-implant marginal bone loss. Clin. Oral Implants Res. 2016, 27,167-173. [CrossRef] [PubMed]
12. Linkevicius, T.; Apse, P.; Grybauskas, S.; Puisys, A. The influence of soft tissue thickness on crestal bone changes around implants: A 1-year prospective controlled clinical trial. Int. J. Oral Maxillofac. Implants 2009, 24, 712-719. [PubMed]
13. Su.rez-L.pez, D.A.F.; Lin, G.H.; Monje, A.; Galindo-Moreno, P.; Wang, H.L. Influence of soft tissue thickness on periimplant marginal bone loss: A systematic review and meta-analysis. J. Periodontol. 2016, 87, 690-699. [CrossRef] [PubMed]
14. Gavira, L.; Salcido, J.P.; Guda, T.; Ong, J.L. Current trends in dental implants. J. Korean Assoc. Oral Maxillofac. Surg. 2014, 40, 50-60. [CrossRef]
15. Preiskel, H.; Tsolka, P. Treatment outcomes in implant therapy: The influence of surgical and prosthodontic experience. Int. J. Prosthodont. 1995, 8, 273-279.
16. Sendyk, D.; Chrcanovic, B.; Albrektsson, T.; Wennerberg, A.; Zindel Deboni, M. Does surgical experience influence implant survival rate? A systematic review and meta-analysis. Int. J. Prosthodont. 2017, 30, 341-347. [CrossRef]
17. Ji, T.; Kan, J.; Rungcharassaeng, K.; Roe, P.; Lozada, J. Immediate loading of maxillary and mandibular implantsupported fixed complete dentures: A 1 to 10 year retrospective study. J. Oral Implantol. 2012, 38, 469-476. [CrossRef]
18. Buser, D.; Weber, H.; Lang, N. Tissue integration of non-submerged implants. 1-year results of a prospective study with
100 ITI hollow-cylinder and hollow-screw implants. Clin. Oral Implants Res. 1990, 1, 33-40. [CrossRef]
19. Albrektsson, T.; Zarb, G.; Worthington, P.; Eriksson, A. The long-term efficacy of currently used dental implants: A review and proposed criteria of success. Int. J. Oral Maxillofac. Implants 1986, 1, 11-25.
20. Beschnidt, S.; Cacaci, C.; Dedeoglu, K.; Hildebrand, D.; Hulla, H.; Iglhaut, G.; Krennmair, G.; Schlee, M.; Sipos, P.; Stricker, A.; et al. Implant success and survival rates in daily dental practice: 5-year results of a non-interventional study using CAMLOG screw-line implants with or without platform-switching abutments. Int. J. Implants Dent. 2018, 33, 33-
46. [CrossRef]
21. Jung, R.; Zembic, A.; Pjetursson, B.; Zwahlen, M.; Thoma, D. Systematic review of the survival rate and the incidence of biological, technical, and aesthetic complications of single crowns on implants reported in longitudinal studies with a mean follow-up of 5 years. Clin. Oral Implants Res. 2012, 23, 2-21. [CrossRef] [PubMed]
22. Pjetursson, B.; Thoma, D.; Jung, R.; Zwahlen, M.; Zembic, A. A systematic review of the survival and complication rates of implant-supported fixed dental prostheses (FDPs) after a mean observation period of at least 5 years. Clin. Oral Implants Res. 2012, 23, 22-38. [CrossRef] [PubMed]
23. Horwitz, J.; Machtei, E.; Frankental, S.; Gabay, E.; Mayer, Y.; Joseph, L.; Cohen, O. Clinical and patient-related outcomes of a tapered implant system with switched platform conical abutments: A private practice field trial. J. Oral Implantol. 2018, 44, 326-329. [CrossRef]
24. Souto, M.J.; Pellizzer, E.; Gomes, J.; Lemos, C.; Santiago Junior, J.; Vasconcelos, B.; Dantes de Moraes, S.L. Influence of diabetes on the survival rate and marginal bone loss of dental implants: An overview of systematic reviews. J. Oral Implantol. 2019, 45, 334-340.
25. Pellicer-Chover, H.; Pe.arrocha-Diago, M.; Pe.arrocha-Oltra, D.; Gomar-Vercher, S.; Agust.n-Panadero, R.; Pe.arrocha-Diago, M. Impact of crestal and subcrestal implant placement in peri-implant bone: A prospective comparative study. Med. Oral Patol. Oral Cir. Bucal 2016, 21, 103-110. [CrossRef]
26. Ercoli, C.; Jammal, G.; Buyers, M.; Tsigarida, A.; Chochlidakis, K.; Feng, C.; Caton, J. Influence of apico-coronal implant placement on post-surgical crestal bone loss in humans. J. Periodontol. 2017, 88, 762-770. [CrossRef]
27. Pellicer-Chover, H.; Pe.arrocha-Diago, M.; Aloy-Prosper, A.; Canullo, L.; Pe.arrocha-Diago, M.; Pe.arrocha-Oltra, D. Does apico-coronal implant position influence peri-implant marginal bone loss? A 36-month follow-up randomized clinical trial. J. Oral Maxillofac. Surg. 2019, 77, 515-527. [CrossRef]
28. Valles, C.; Rodriguez-Ciurana, X.; Mu.oz, F.; Permuy, M.; L.pez-Alonso, H.; Nart, J. Influence of implant neck surface and placement depth on crestal bone changes and soft tissue dimensions around platform-switched implants: A histologic study in dogs. J. Clin. Periodontol. 2018, 45, 869-883. [CrossRef]
29. Souza, A.; Tormena, M.; Matarazzo, F.; Ara.jo, M. The influence of peri-implant keratinized mucosa on brushing discomfort and peri-implant tissue health. Clin. Oral Implants Res. 2016, 27, 650-655. [CrossRef]
30. Ladwein, C.; Schmelzeisen, R.; Nelson, K.; Fluegge, T.; Fretwurst, T. Is the presence of keratinized mucosa associated with peri-implant tissue health? A clinical cross-sectional analysis. Int. J. Implants Dent. 2015,1, 11-24. [CrossRef]
31. Perussolo, J.; Souza, A.B.; Matarazzo, F.; Oliveira, R.; Ara.jo, M. Influence of the keratinized mucosa on the stability of peri-implant tissues and brushing discomfort: A 4-year follow-up study. Clin. Oral Implants Res. 2018, 29, 1177-1185. [CrossRef] [PubMed]
32. Canullo, L.; Pen.rrocha-Oltra, D.; Covani, U.; Botticelli, D.; Serino, G.; Penarrocha, M. Clinical and microbiological findings in patients with peri-implantitis: A cross-sectional study. Clin. Oral Implants Res. 2016, 27, 376-382. [CrossRef] [PubMed]
33. Schwarz, F.; Becker, J.; Civale, S.; Sahin, D.; Iglhaut, T.; Iglhaut, G. Influence of the width of keratinized tissue on the development and resolution of experimental peri-implant mucositis lesions in humans. Clin. Oral Implants Res. 2018, 29, 576-582. [CrossRef] [PubMed]
34. Roccuzzo, M.; Grasso, G.; Dalmasso, P. Keratinized mucosa around implants in partially edentulous posterior mandible: 10-year results of a prospective comparative study. Clin. Oral Implants Res. 2016, 27, 491-496. [CrossRef]
35. Wennstr.m, J.; Derks, J. Is there a need for keratinized mucosa around implants to maintain health and tissue stability? Clin. Oral Implants Res. 2012, 23, 136-146. [CrossRef]
36. Lin, G.; Madi, I. Soft-Tissue conditions around dental implants: A literature review. Implants Dent. 2019,28, 138-143. [CrossRef]
37. Canullo, L.; Camacho-Alonso, F.; Tallarico, M.; Meloni, S.; Xhanari, E.; Penarrocha-Oltra, D. Mucosa thickness and peri-implant crestal bone stability: A clinical and histologic prospective cohort trial. Int. J. Oral Maxillofac. Implants 2017, 32, 675-681. [CrossRef]
38. Linkevicius, T.; Puisys, A.; Steigmann, M.; Vindasiute, E.; Linkeviciene, L. Influence of Vertical soft tissue thickness on crestal bone changes around implants with platform switching: A comparative clinical study. Clin. Implants Dent. Relat. Res. 2015, 17, 1228-1236. [CrossRef]
39. Galindo-Moreno, P.; Le.n-Cano, A.; Ortega-Oller, I.; Monje, A.; Su.rez, F.; .Valle, F.; Spinato, S.; Catena, A. Prosthetic abutment height is a key factor in peri-implant marginal bone loss. J. Dent. Res. 2014, 93, 80-85. [CrossRef]
40. Spinato, S.; Stacchi, C.; Lombardi, T.; Bernardello, F.; Messina, M.; Zaffe, D. Biological width establishment around dental implants is influenced by abutment height irrespective of vertical mucosal thickness: A cluster randomized controlled trial. Clin. Oral Implants Res. 2019, 30, 649-659. [CrossRef]
41. Chen, Z.; Lin, C.; Li, J.; Wang, H.; Yu, H. Influence of abutment height on peri-implant marginal bone loss: A systematic review and meta-analysis. J. Prosthet. Dent. 2019, 122, 14-21. [CrossRef] [PubMed]
2020 Авторы Лицензиат MDPI, Базель, Швейцария Данная статья является материалом с открытым доступом и распространяется на условиях лицензии Creative Commons Attributio (CC BY) (http://creativecommons.org/licenses/by/4.0/).