Наименование медицинского изделия:
Имплантат зубной с коническим соединением, в комплекте с фрезой конической.
Варианты исполнения:
Имплантат зубной C1 с коническим соединением, в комплекте с фрезой конической, компонентом временным и заглушкой:
C1-10330, C1-11330, C1-13330, C1-16330, C1-08375, C1-10375, C1-11375, C1-13375, C1-16375, C1-08420, C1-10420, C1-11420, C1-13420, C1-16420, C1-08500, C1-10500, C1-11500, C1-13500, C1-16500.
В составе:
1. Имплантат зубной — 1 шт.
2. Заглушка — 1 шт.
3. Фреза коническая — 1 шт.
4. Компонент временный (включая винт ортопедический) — 1 шт.
5. Этикетка отслеживаемости — 3 шт.
6. Инструкция по применению — 1 шт.
Имплантат зубной V3 с коническим соединением, в комплекте с фрезой конической и заглушкой:
V3-10330, V3-11330, V3-13330, V3-16330, V3-08390, V3-10390, V3-11390, V3-13390, V3-16390, V3-08430, V3-10430, V3-11430, V3-13430, V3-16430, V3-08500, V3-10500, V3-11500, V3-13500, V3-16500.
В составе:
1. Имплантат зубной — 1 шт.
2. Заглушка — 1 шт.
3. Фреза коническая — 1 шт.
4. Этикетка отслеживаемости — 3 шт.
5. Инструкция по применению — 1 шт.
Далее по тексту – «Имплантаты зубные MIS», «Имплантаты MIS», «Имплантат»; а также под «сопутствующие компоненты» подразумеваются, входящие в комплект поставки «заглушка» и «компонент временный (включая винт ортопедический»).
| Комплектность поставки имплантата | В варианте исполнения имплантата | Материал изготовления | |
| C1 | V3 | ||
| Имплантат зубной | 1 шт | 1 шт | Титановый сплав Ti 6Al 4V ELI (стандарт ASTM F136) |
| Заглушка | 1 шт | 1 шт | Титановый сплав Ti6Al4V ELI (стандарт ASTM F136) |
| Фреза коническая | 1 шт | 1 шт | Сталь нержавеющая, 1.4197, Chronifer® Labor M-Plus (SS_420F) |
| Компонент временный (включая винт ортопедический) | 1 шт | — | Полиэфирэфиркетон, натуральный непрозрачныйPEEK, (винт ортопедический: Титановый сплав Ti 6Al 4V ELI (стандарт ASTM F136) |
| Этикетка отслеживаемости | 3 шт | 3 шт | Бумага самоклеящаяся |
| Инструкция по применению | 1 шт | 1 шт | Бумага |
Показания к применению
Показаниями к зубной имплантации являются такие изменения зубов и их опорного аппарата, как:
- дефекты зубного ряда,
- полное отсутствие зубов,
- невозможность использования съемного протеза.
Имплантаты зубные MIS предназначены для установки методом хирургического вмешательства в костную ткань верхней и нижней челюсти с целью поддержки ортопедических конструкций, таких как искусственные зубы, и восстановления жевательной функции. После одноэтапной установки имплантата возможна и немедленная нагрузка, если достигнуты хорошая первичная стабильность и приемлемая окклюзия (определение стабильности имплантата и приемлемости окклюзии осуществляется в соответствии с принятыми в медицинском учреждении методиками). Узкие имплантаты (Ø3,3мм) показаны в хирургии и протезировании для установки только на участках центральных и боковых резцов нижней челюсти и боковых резцов верхней челюсти с частичным отсутствием зубов для создания опоры для ортопедической конструкции, например, искусственных зубов. Центральные и боковые резцы верхней челюсти следует связывать в единую конструкцию, если используется два или более узких имплантата, расположенных подряд.
Назначение и принципы действия
Имплантаты MIS, представляющие собой опорную часть в виде резьбового винта, предназначены для хирургической установки врачом-стоматологом в костную ткань верхней и нижней челюсти пациента с целью закрепления или поддержки искусственных зубов и восстановления жевательной и эстетической функции.
Информация о потенциальных потребителях медицинского изделия:
- отделения медицинских учреждений направления Стоматология,
- медицинские учреждения направления Стоматология,
- врачи-стоматологи.
Функциональные характеристики и назначение, описание принадлежностей и медицинских изделий, предусмотренных для использования в комбинации с имплантатами
Имплантаты MIS – это самонарезающие, корневидные, двухкомпонентные винтовые зубные имплантаты, изготовленные из титанового сплава. Импланты MIS С1 в верхней трети имплантата имеют круглую форму, а V3 — некруглую форму в виде треугольника с закругленными краями. Имплантаты MIS V3, имеющие некруглую форму, отличаются наличием плоских поверхностей в пришеечной области , что позволяет его эффективно использовать у пациентов с узким альвеолярным гребнем в большом количестве случаев, не применяя остеотомическую технику, располагая плоскости треугольника в соответствии с направлением костного гребня, параллельно стороне треугольника. Имплантаты MIS предназначены для использования в сочетании с винтами-заглушками, формирователями десны, ортопедическими компонентами, такими как: стандартными абатментами, в т.ч. с углом наклона до 25° и дополнительными абатментами для фиксации коронки. Использование ортопедических компонентов и принадлежностей, изготовленных специально для имплантатов MIS, обеспечивает максимальную совместимость и точность.
Во время выполнения хирургической манипуляции с имплантатом зубным обязательно применение хирургических стерильных перчаток.
При эксплуатации Имплантат зубной с коническим соединением, в комплекте с фрезой конической и сопутствующими компонентами устойчивы к воздействию температуры от 32 до 42˚С, относительной влажности 100 % и воздействиям биологических жидкостей и выделений тканей организма, с которыми они контактируют в процессе эксплуатации.
В комплект поставки к каждому имплантату входит фреза коническая и сопутствующие компоненты соответствующих этому имплантату размеров и геометрических параметров. Соответствие геометрических параметров фрезы геометрическим параметрам имплантата, с которым она поставляется, позволяет избежать перегрузки кости при установке имплантата для обеспечения как лучшего результата остеоинтеграции, так и лучшего результата имплантологического лечения в целом. Использование для подготовки имплантационного ложа на финальном этапе фрез другого размера и формы, запрещается.
Необходимые для установки имплантата инструменты и последующие ортопедические компоненты (в т.ч. абатменты) и принадлежности к ним поставляются отдельно от имплантатов.
Описание упаковки
Имплантат помещен в защитную титановую втулку, препятствующую загрязнению поверхности имплантата материалами упаковки. Втулка с имплантатом размещена во внутренней колбе, в крышке которой расположена заглушка соответствующего имплантату типоразмера. Вместе с этикетками отслеживаемости внутренняя колба помещена во внешнюю колбу с завинчивающейся крышкой. Фреза имеет индивидуальную упаковку. Компонент временный, включая винт ортопедический, имеет индивидуальную упаковку. Колба с имплантатом, этикетками отслеживаемости и заглушкой, пакет с фрезой, пакет с компонентом временным упакованы в картонную коробку и сопровождаются инструкцией. Картонная коробка запечатана с обоих торцов прозрачными стикерами. Имплантат может поставляться в групповых упаковках из картона по 10 штук одного типоразмера (для варианта C1) и по 4 шт или 10 штук (для варианта V3). Групповая картонная коробка (пенал) запечатана стикером с соответствующей маркировкой.
Материалы изготовления упаковки: титановый сплав группы VIII (втулка); полистирол и полипропилен (колбы); полиэтилентерефталат/алюминиевая фольга/полиэтилен PETMET/PE, PET/PE (пакет фрезы и компонента временного); картон (коробка индивидуальная и групповая).
Технические характеристики (гарантированные производителем (изготовителем) значения основных параметров)
- Имплантаты MIS изготавливаются из биосовместимого титанового сплава, их поверхность обрабатывается пескоструйно и протравливается кислотой с целью создания шершавости, имитирующей фактуру костной ткани.
- Имплантаты MIS выпускаются в нескольких типоразмерах, различающихся диаметрами, длиной и соответствующим типоразмером платформы (узкая NP, стандартная SP и широкая WP).
- Тип соединения имплантата для последующей установки принадлежностей или ортопедических конструкций — коническое (синоним «конусное») 12˚, с антиротационным компонентом.
Таблицы соответствия типоразмеров и номеров по каталогу:
— для варианта исполнения C1:
| L
D |
Цветовая кодировка | платформа | 8мм | 10мм | 11.5мм | 13мм | 16мм |
| 3.30мм | Желтый | NP | — | C1-10330 | C1-11330 | C1-13330 | C1-16330 |
| 3.75мм | Фиолетовый | SP | C1-08375 | C1-10375 | C1-11375 | C1-13375 | C1-16375 |
| 4.20мм | C1-08420 | C1-10420 | C1-11420 | C1-13420 | C1-16420 | ||
| 5.0мм | Зеленый | WP | C1-08500 | C1-10500 | C1-11500 | C1-13500 | C1-16500 |
— для варианта исполнения V3:
| L
D |
платформа | 8мм | 10мм | 11.5мм | 13мм | 16мм | |
| 3.30мм | Синий | NP | — | V3-10330 | V3-11330 | V3-13330 | V3-16330 |
| 3.90мм |
Фиолетовый |
SP |
V3-08390 | V3-10390 | V3-11390 | V3-13390 | V3-16390 |
| 4.30мм | V3-08430 | V3-10430 | V3-11430 | V3-13430 | V3-16430 | ||
| 5.0мм | V3-08500 | V3-10500 | V3-11500 | V3-13500 | V3-16500 |
Цветовое кодирование типоразмера платформы обеспечивается оптическими свойствами пленки оксида титана, полученной путем электрохимического анодирования поверхности без применения красителей. Цветовое кодирование типоразмера платформы имплантатов, ортопедических компонентов (в том числе абатментов) и принадлежностей к ним предназначено для быстрой визуальной идентификации врачом-стоматологом соответствия комбинаций указанных медицинских изделий и инструментов для их установки. Наличие цветового кода на изделии и/или его упаковке не освобождает пользователя от ответственности за проверку типоразмера по маркировке.
Имплантаты MIS не содержат лекарственных средств, материалов животного и (или) человеческого происхождения.
Стерилизация
Содержимое упаковки с имплантатом MIS и входящими в комплект поставки фрезами и сопутствующими компонентами стерилизовано гамма-облучением.
Важно
Врачи-стоматологи должны следовать соответствующим протоколам установки и нагрузки с целью достижения хорошей начальной стабильности и соответствующей окклюзионной нагрузки, в особенности при применении процедуры немедленной нагрузки. На предоперационном этапе необходимо выполнить определение высоты и ширины доступной костной ткани. С помощью рентгенографии необходимо оценить доступность костной ткани, оптимальное местоположение установки имплантата и его типоразмера (диаметр, длина) без повреждения таких структур, как кровеносные сосуды, нервы, нижнечелюстной канал, верхнечелюстные пазухи, мягкие ткани и соседние зубы. Рекомендуемый вращающий момент при вкручивании: 35-60 Нсм. Избегайте чрезмерных усилий при установке имплантата в костную ткань.
Противопоказания
Необходимо принимать во внимание обычные противопоказания к хирургическим операциям в полости рта при работе с другими имплантируемыми материалами. Это прием пациентами кортикостероидов или противосудорожных средств, а также прохождение радиационной терапии или иных видов иммуносупрессивного лечения. Не следует применять у пациентов с отклонениями лабораторных показателей АМК, уровня креатинина или кальция в сыворотке, у пациентов с диабетом, сердечно-сосудистыми заболеваниями, гипертензией с уровнем артериального давления свыше 170/110 мм рт. ст., трещинами костей вследствие остеопороза, заболеваниями органов дыхания, заболеваниями щитовидной железы, а также у пациентов с диагностированными в течение последних пяти лет злокачественными новообразованиями, увеличенными лимфатическими узлами, болезненностью или опухолями неизвестной этиологии в области головы и шеи. Процедуры имплантации не следует применять у пациентов с активными остеолитическими, воспалительными или инфекционными процессами в месте имплантации.
Использование имплантатов противопоказано при:
- инвалидизирующих и неконтролируемых заболеваниях;
- гемофилии, гранулоцитопении или иных заболеваниях, сопровождающихся кровотечениями, применении стероидных препаратов, профилактическом применении антибиотиков, лабильном диабете 1-го типа;
- синдроме Элерса-Данлоса;
- остеорадионекрозе, почечной недостаточности, пересадке органов, антикоагуляционной терапии, идиопатической гиперчувствительности, фиброзной дисплазии, регионарном энтерите;
- недостаточного уровня подготовки медицинского работника;
- состояниях, заболеваниях или видах терапии, которые могут серьезно нарушить процесс заживления, например, радиационная терапия;
- слабой мотивации пациента;
- психических расстройствах, негативно влияющих на взаимопонимание с пациентом и выполнение пациентом необходимых требований и процедур;
- несоответствии ожиданий пациента реальному положению вещей;
- невозможности реконструкции путем протезирования;
- неспособности пациента соблюдать требования гигиены ротовой полости;
- гиперчувствительности пациента к материалам определенных частей имплантатов.
Риски применения, ожидаемые и предсказуемые побочные эффекты
Риски, связанные с хирургическими процедурами, можно разделить на несколько широких категорий:
- Немедленные риски, связанные с анестезией и хирургическим вмешательством.
- Психологические и психиатрические риски.
- Медицинские риски и долговечность имплантатов.
- Вредное воздействие имплантатов на состояние здоровья в долгосрочной перспективе.
Риски могут включать:
- непреднамеренную перфорацию носовых или верхнечелюстных пазух, местные и системные инфекции, перфорацию окружающих мягких тканей, повреждение нервов;
- временные состояния, связанные с установкой имплантатов, могут включать боль и отеки, проблемы с речью и гингивит;
- в долгосрочной перспективе возможны повреждения нервов, местные или системные бактериальные инфекции, а у восприимчивых лиц – также инфекционный эндокардит;
- существующий естественный зубной ряд может быть нарушен вследствие неправильной установки имплантатов.
Риск может возрастать при наличии следующих патофизиологических нарушений в соответствующих системах органов:
- Сердечно-сосудистая система: коронарная болезнь, аритмии
- Дыхательная система: хроническое обструктивное заболевание легких
- Желудочно-кишечный тракт: гепатит, мальабсорбция, воспалительное заболевание кишечника
- Мочеполовая система: хроническая почечная недостаточность
- Эндокринная система: диабет, заболевания щитовидной железы, нарушения гипофиза или надпочечников
- Кровеносная система: анемия, лейкемия, нарушения свертывания
- Опорно-двигательный аппарат: артрит, остеопороз
- Неврологические нарушения: инсульт, паралич, умственная отсталость.
Важное предостережение
- Недостаточный уровень подготовки медицинского работника является основным фактором риска при установке имплантатов и может представлять угрозу здоровью пациента. Поэтому процедуры установки имплантатов должны выполняться только в условиях лечебно-профилактических учреждений, имеющих лицензию на хирургическое лечение в стоматологии, и при наличии у медицинского работника соответствующего профессионального образования, а также действующей медицинской лицензии/сертификата, разрешающего хирургические манипуляции.
- Во избежание повреждения существующего зубного ряда и/или других имплантатов расстояние между имплантатами должно быть не менее 2 мм.
- Имплантаты MIS не проходили оценку на безопасность и совместимость с исследованием МРТ. Они не проходили оценку на нагрев, миграцию или создание артефактов в среде МРТ. Безопасность конических имплантатов MIS при проведении обследования МРТ неизвестна. Сканирование пациента, которому установлены такие имплантаты, может привести к травме.
- Имплантаты малого диаметра и угловые абатменты не рекомендуются для установки в дистальной области.
Меры предосторожности
- Имплантат MIS и входящие в комплект поставки фреза коническая и сопутствующие компоненты предназначены для одноразового использования.
- Не использовать Имплантаты MIS и входящие в комплект поставки фрезы и сопутствующие компоненты при повреждении стерильной упаковки.
ЗАПРЕЩАЕТСЯ ПОВТОРНАЯ СТЕРИЛИЗАЦИЯ и/или повторное использование имплантатов и входящих в комплект поставки фрез и сопутствующих компонентов. Повторное использование запрещено: компания MIS требует строго придерживаться принципа одноразового использования зубных имплантатов и никогда не использовать их повторно. Повторное использование может стать причиной инфекций, резорбции кости, повреждения твердых и мягких тканей и/или неудачи при установке имплантатов. Успех установки имплантата и его остеоинтеграция прямо связаны с чистотой поверхности, отсутствием каких бы то ни было биологических или иных загрязнений на поверхности и уровнем стерильности.
- Установка имплантата может потребовать предварительной профилактической терапии антибиотиками.
- При использовании имплантатов MIS дополнительная обработка поверхности не требуется.
- Не превышайте максимально допустимую скорость препарирования. Обеспечьте достаточную ирригацию фрезы. Сведение к минимуму травматичности для кости и окружающих тканей повышает шансы на успешную остеоинтеграцию.
Информация для проверки правильности имплантации
Проверка правильности имплантации обеспечивается и осуществляется в соответствии с принятыми в медицинском учреждении методиками с использованием различных типов рентгенограмм и технологий визуализации как в предоперационном периоде планирования, так и во время и после хирургического вмешательства.
В качестве мероприятий по обеспечению и проверке правильности имплантации рекомендуется:
- промежуточная проверка правильности препарирования костного ложа под имплантат с помощью глубиномера,
- применение на финальной стадии препарирования костного ложа фрезы конической, поставляемой с имплантатом и соответствующей ему по геометрическим параметрам.
Имплантаты MIS являются стерильными изделиями для одноразового применения и не подлежат ремонту и/или техническому обслуживанию.
Нет достаточно исследований на предмет выживаемости установленных пациентам имплантатов зубных сроком свыше 20 лет. Тем не менее, систематическая гигиена полости рта и регулярные визиты к врачу-стоматологу, а также избегание таких вредных привычек как курение, смогут способствовать продлению срока службы имплантата.
Гарантия
Имплантаты MIS и входящие в комплект поставки фрезы и сопутствующие компоненты – изделия одноразового использования. Срок годности ограничен и составляет 5 лет с даты изготовления. Дата истечения срока годности указана на упаковке («Использовать до») и действительна при соблюдении условий транспортировки и хранения.
Ограниченная гарантия
В случае отторжения имплантата компания MIS осуществляет его бесплатную замену при выполнении следующих условий: письменное уведомление компании MIS о неудаче установки имплантата не позднее чем через 6 месяцев после появления первых признаков такой неудачи, предоставление отчета по форме, предоставляемой MIS (см. «Протокол врачебного наблюдения за имплантатом» на сайте http://www.misrussia.ru), соответствующих рентгенографических снимков и самого имплантата. Это полная гарантия имплантата, предоставляемая компанией MIS, при условии проведения медикаментозного лечения, показанного для процедуры имплантации.
Условия транспортировки и хранения.
Имплантаты MIS транспортируются всеми видами транспорта в крытых транспортных средствах в соответствии с действующими на данном виде транспорта правилами перевозок при температуре от -25˚ до +55˚ С и относительной влажности воздуха 40-90%. Во всех случаях транспортировки продукция должна быть уложена плотно, а свободные места заполнены.
Имплантаты MIS подлежат хранению в оригинальной упаковке в условиях складских помещений при температуре от +5 до +40 ˚С и относительной влажности воздуха 40-90%, не допускать воздействия прямого солнечного света и следить за целостностью упаковки.
Предосторожности при утилизации
Использованные и/или бывшие в употреблении имплантаты MIS и входящие в комплект поставки фрезы конические и сопутствующие компоненты относятся к классу эпидемиологически опасных отходов (инфицированные или потенциально инфицированные отходы: материалы и инструменты, предметы, загрязненные кровью и/или другими биологическими жидкостями). Следуйте национальному или локальному законодательству по уничтожению медицинских отходов.
| Разъяснение использованных символов и сокращений | |
 |
Для одноразового использования |
 |
Стерилизовано гамма-облучением |
 |
Не стерилизовать повторно |
 |
Использовать до |
 |
Код партии |
 |
Номер по каталогу |
 |
Производитель (Изготовитель) |
 |
Дата производства (изготовления) |
 |
Не допускать воздействия солнечного света |
 |
Не использовать при повреждении упаковки |
 |
Осторожно! Обратитесь к инструкции по применению |
 |
Обозначение соответствия при обязательном декларировании соответствия в системе ГОСТ Р |
 |
Предостережение: Федеральный Закон США разрешает продажу этого изделия только стоматологам или по их заказу. |
 |
Уполномоченный представитель в Европейском сообществе |
 |
Обозначение соответствия требованиям директив и стандартов Европейского союза |
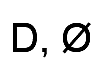 |
Диаметр (мм) |
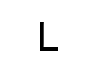 |
Длина (мм) |
 |
Узкая платформа |
 |
Стандартная платформа |
 |
Широкая платформа |
 |
Индикатор стерилизации на групповой упаковке (красный цвет = стерилизовано) |
 |
Производитель (изготовитель): «МИС Имплантс Технолоджис Лтд.», Израиль (P.O. Box 7, Bar Lev Industrial Park 2015600, Israel Тел.: +972 (0)4 90 16 800 service@mis-implants.com |
 |
Товарный знак предприятия-изготовителя |
Перечень применяемых производителем (изготовителем) медицинского изделия национальных стандартов:
Производство соответствует требованиями стандарта серии ISO 13485; в отношении продукции применяются стандарты серий: ISO 10993, ISO 14971, ISO 14801, ISO 1797, ISO 10271, ISO 5832-3, ISO 11607-1, ISO 15223-1. Для получения актуальной информации о подтверждении соответствия обязательным требованиям обратитесь к уполномоченному представителю производителя на территории обращения медицинского изделия.
Данная версия инструкции по применению MP-UI101-C1V3_RUS Rev.1 (2019-01, первичный выпуск), утверждена компанией производителем «МИС Имплантс Технолоджис Лтд.» (Израиль) для обращения медицинского изделия на территории Российской Федерации и предоставляется уполномоченным представителем производителя (вместе с Имплантатами MIS) на бумажном носителе и в форме электронного документа посредством размещения в информационно-телекоммуникационной сети Интернет по адресу http://www.misrussia.ru. Международная версия инструкции по применению MP-UI101 Rev.2 (August 2018) поставляется на бумажном носителе, вложенном в картонную коробку каждой единицы изделия.
Смотри также:
Приложение 1 — Хирургическое руководство (рекомендованные хирургические протоколы).
Приложение 2 — Протокол врачебного наблюдения за имплантатом (уведомление компании MIS о неудаче установки имплантата PDF файл).
Приложение 3 — Рекомендации пациенту по уходу за полостью рта в постоперационный период после установки зубного имплантата.
